マネジメントブログ
2019年6月期決算説明会を開催しました
本日10時から、例年どおり東京丸の内・三菱ビルのカンファレンススクエアエムプラスで、アナリスト向け決算説明会を開催しました。
配布資料は既にTDNETと当社ウェブサイトに掲載しています。
プレゼンテーションの動画や質疑応答テキスト書き起こしは、このブログポストの時点ではまだ掲載されていませんが、数日中にアップロードされるはずです。
臨床試験の進捗状況については、適時開示の基準に該当することが少なく、こういった説明会の機会にお話しする情報や質疑応答が中心になります。
今回はちょうどCBP501フェーズ1b拡大相試験の真っ最中ということで、アナリストの皆さんやメディアの方のご注目やご質問がそこに集中することが想定されました。
そのため、今回はいつもの2部構成(決算報告・事業報告)に加え、Part 3 として「CBP501概況報告 〜臨床試験、今後の動き」を独立させ、しっかり時間をかけてお伝えすることにしました。
このPart 3 については動画を御覧ください…
と申し上げるべきところなのですが、なかなか見ていただけません(実際、残念なのですが過去の動画も、最後まで見ていただける率はあまり高くありません)。
かといって、資料の字づらだけを追われると、むやみな誤解も生みかねません。
そこで今回はさらに一計を案じ、概ね1スライド1ツイートにまとめ直して、ツイッターで概略を公表することにしました。
今日のブログでは、そのツイート集をお読みいただくことにします。
(ツイッターアカウントをお持ちの方は、こちらのリンクからツイッター画面でスレッドを読んでいただくほうが読みやすいと思います)

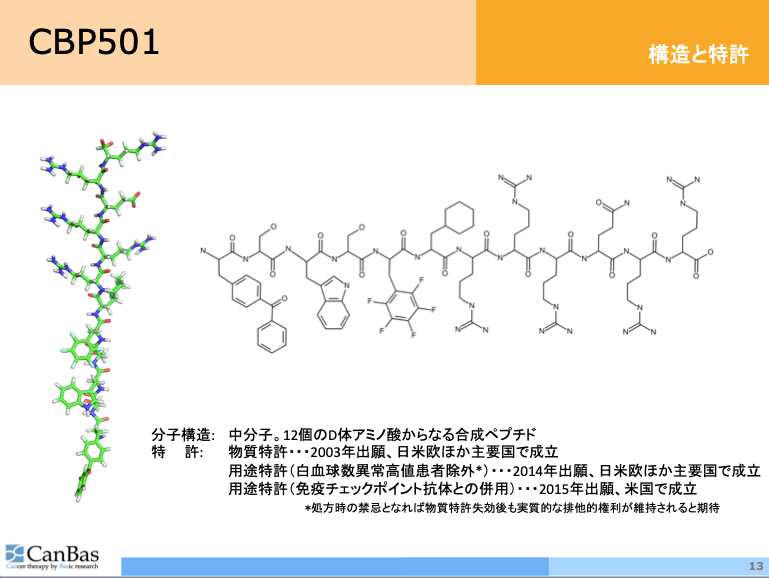
物質特許は2003年出願でこのままでは特許寿命の短さが懸念されるところですが、白血球異常値の患者を除外する用途特許(日米欧で成立)などで実質的な排他的権利期間の延伸を図っています。

中でも、癌細胞の免疫原性細胞死を増やす作用とM2マクロファージの働きを抑制する作用は、免疫系抗癌剤との併用において重要な意味を持つと考えています。
また併用するシスプラチンの効果を増強し悪い部分を改善すると考えています。
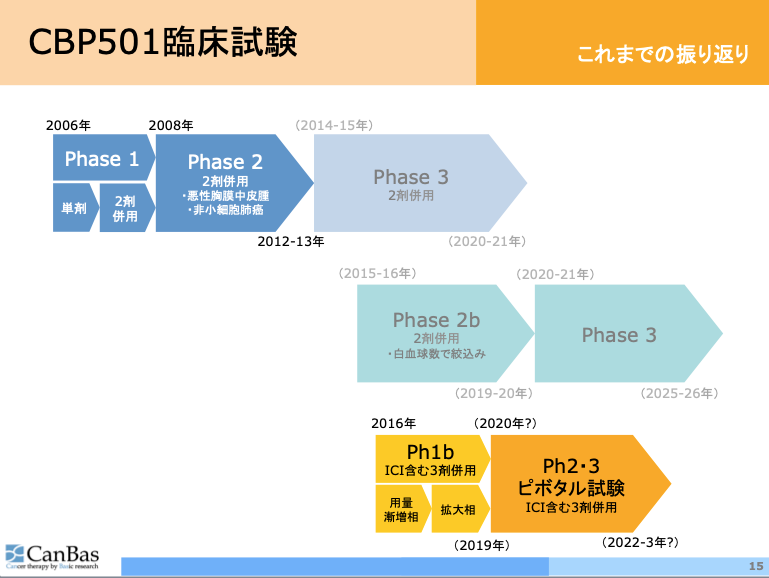
薄い色の矢印は実施しなかった臨床試験計画です。
現在は右下のオレンジ色の臨床試験をフェーズ1b拡大相途中まで進めています。

用量漸増相の好感触等を踏まえ、拡大相は対象を治療抵抗性(過去の治療が効かなくなった)の膵臓癌とMSS直腸大腸癌(MSSはステージIV直腸大腸癌の大半)に絞って現在実施中です。
安全性の懸念は現在までのところありません。

過去の多数の臨床試験において免疫チェックポイント抗体による奏効がほぼゼロとわかっている対象で、複数の奏効や病勢コントロールが確認できています。

特に膵臓癌とMSS直腸大腸癌については、ヒストリカル(過去の臨床試験データ)と比べて注目に値する結果です。
まだ少数例なので強くは言えないものの、好感触であるとは言えます。
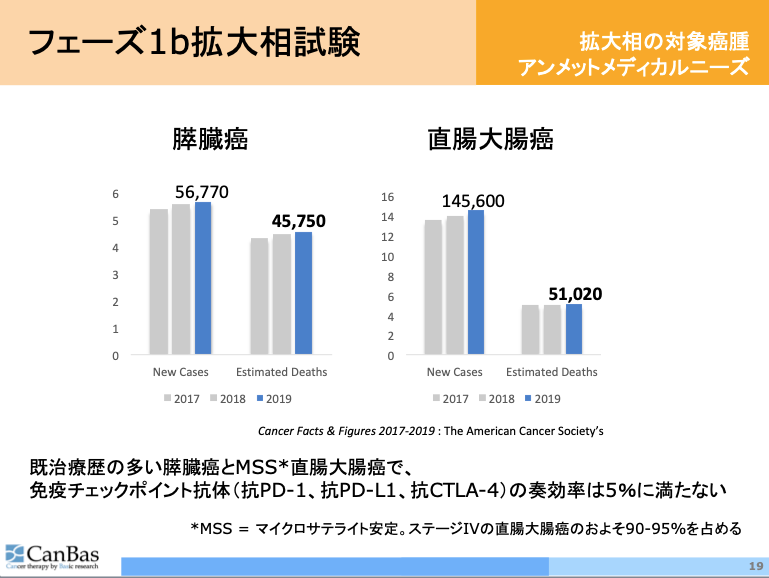
直腸大腸癌は数の多さ、膵臓癌は新規診断数と死亡数の差の小ささが特徴です。
注目の免疫チェックポイント抗体をもってしても既治療歴の多い膵臓癌とMSS直腸大腸癌では奏効率5%に満たず、いずれも大きなアンメットメディカルニーズがあります。
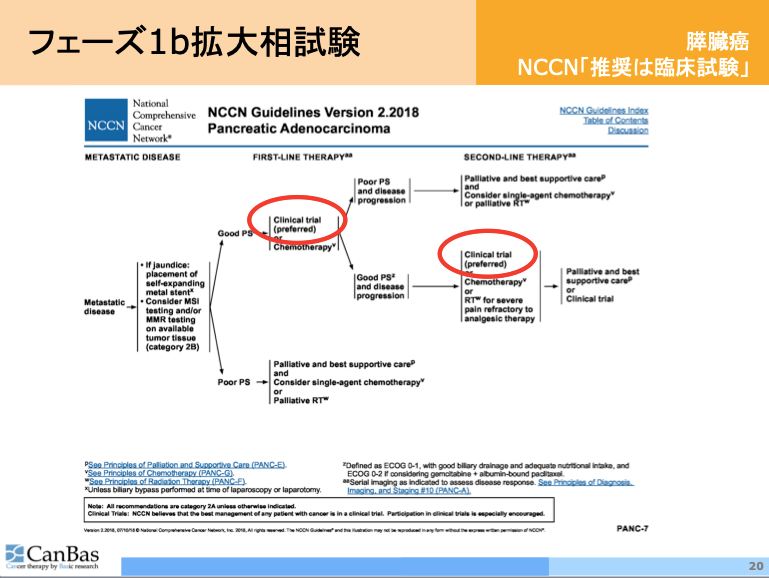
ご覧のとおり、転移のある膵臓癌の一次治療については
「化学療法もあるが、臨床試験への参加が望ましい」
とガイドラインが推奨しているのが現状です。

報道等で持つ印象とは裏腹に、免疫チェックポイント抗体を使った臨床試験で後期まで残っているものは多くありません。
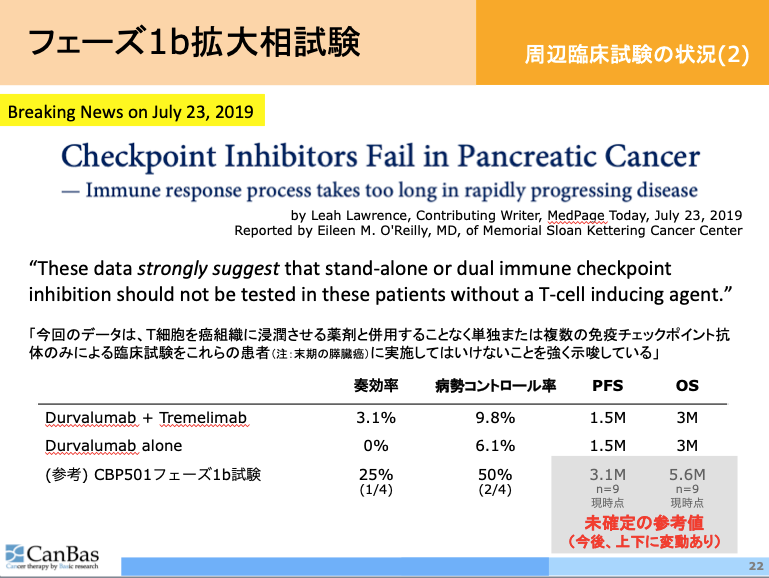
免疫チェックポイント抗体を使った膵臓癌の大規模臨床試験の失敗を受け、
「単独または複数の免疫チェックポイント抗体『のみ』による臨床試験はやめるべき」
と厳しく指摘しています。
比較のためCBP501の現時点まで(拡大相を一部含みます)の参考値を並べました。
なお、この図のCBP501の値は症例数の少ないあくまでも参考値であり、しかも未だ変動(上下とも)の余地があります。
野球の開幕カードで3連勝して「優勝や」と思ってしまうようなことが臨床試験ではよくあるので、あくまでも「好感触とキャンバスが言っている根拠」としてご覧ください。

奏効や病勢コントロールの具体的な数値は未だ公表を差し控えますが、前の図でご覧いただいたように好感触ではあります。
また、まだ少数例の結果ですが採取した組織の免疫染色による薬力学的評価でも、想定している作用機序を支持する分析結果を得ています。
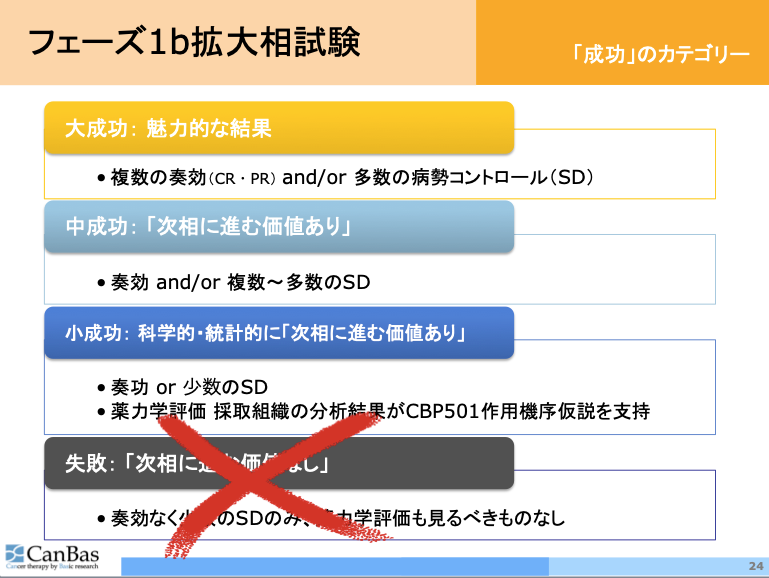
誰が見ても大成功(複数の奏効and/or多数のSD)のほか、
客観的にも次相臨床試験に進む価値ありと見られる「中成功」、
第三者のビジネス判断は難しいかもしれないものの医学的科学的に次相臨床試験に進む価値を主張し得る「小成功」
があり得ます。
どれにも当てはまらない結果に終わった場合、今回の試験は「失敗」です。
しかし幸いなことに現時点までのデータから、少なくとも箸にも棒にも掛からぬ「失敗」に終わる心配はなくなりました。
したがって今後の展開シナリオは、「成功」の内容次第で開発戦略や提携戦略が分岐していくことになります。

現在の順調な組入れ状況が続けば、2019年9-12月に各癌腫の組入れ完了を開示することになります。
中間とりまとめの実施有無は未定ですが、するとすれば2020年前半になります。
拡大相のデータに関する学会発表は、現在の順調な組入れ状況が続けば、2020年6〜9月になると予想されます。
また、当然ですがそれら以外のニュースがまったくないわけではなく、例えば(あくまで例ですが)良くも悪くもとてつもないデータが出るなどした場合にはもちろん随時公表します。
記事を探す
- 未分類
カテゴリーから探す
タグから探す
- 学会発表
- 企業価値
- 競合
- 基礎研究
- 説明会
- 会社紹介
- マスメディア報道
- 余談
- 採用
- 加登住
- 提携獲得活動
- ご挨拶
- 臨床試験
- サイエンス
- 河邊
- 質疑応答
- ファイナンス
- 近況
- 適時開示
- 業界知識
- 決算説明
- 学会
- 日比野
- 決算
- 株主価値
- 株主総会
- 臨床開発
- お詫び
著書から探す
新着記事一覧
2023.12.29
2023.10.24
2023.10.16
2023.10.01
2023.09.27
よく読まれている記事
2023.02.24
2022.11.05
2023.12.29
2023.10.24
2022.09.07